Lécithine de soja raffinée (qualité pharmaceutique)
Brève introduction aux phospholipides :
Les phospholipides sont un type de lipides contenant du phosphore, notamment les glycérophospholipides et la sphingomyéline. Les glycérophospholipides sont largement répandus chez les animaux, les plantes et les micro-organismes, tandis que les sphingomyélines ne sont généralement présentes que chez les animaux et les micro-organismes, et sont extrêmement rares chez les plantes. Les phospholipides courants désignent principalement les glycérophospholipides, tels que les phospholipides végétaux (phospholipides de soja, de colza, de coton, etc.) et les phospholipides de jaune d'œuf, dont les principaux composants sont la phosphatidylcholine (PC), la phosphatidyléthanolamine (PE) et le phosphatidylinositol (PI).
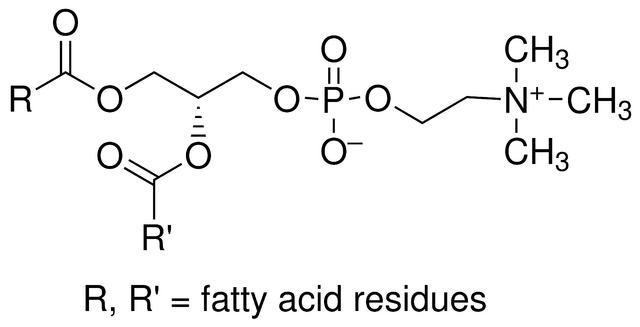
Le nom chimique de la lécithine est phosphatidylcholine (PC). Selon sa pureté, elle est généralement divisée en PC50, PC60, PC70, PC80, PC90, PC95 et autres formes de produits. La pureté maximale peut atteindre 98 %. Plus la pureté est élevée, plus la performance d'oxydation est élevée. La lécithine purifiée à 98 % doit donc être hydrogénée avant conservation. La lécithine non hydrogénée doit généralement être conservée dans un récipient hermétique rempli d'azote.
À température ambiante, la lécithine pure est un solide blanc incolore et inodore. En réalité, elle peut varier de jaune clair à brun en raison des différentes méthodes de préparation ou de raffinage et des conditions de stockage.
Lécithine de soja de qualité pharmaceutique ordinaire :
La lécithine de soja de qualité pharmaceutique (phosphatidylcholine, appelée PC) est un produit cireux jaune fabriqué à partir de lécithine de poudre de soja comme matière première, extraite à l'éthanol et par d'autres procédés à l'aide d'équipements brevetés (ZL2017.20049599.7 ; ZL2010.20147413.X). Ses principales spécifications sont les PC-50 et PC-70.
Spécifications du produit :
| Indicateurs physiques et chimiques | ||
| PC-50 | PC-70 | |
| Apparence | Solide cireux jaune | |
| Phosphore (P) | ≥ 2,7 % | ≥ 2,7 % |
| Azote (N) | 1,5%~2,0% | 1,5%~2,0% |
| Phosphatidylcholine (PC) | ≥ 45,0 % | ≥ 70,0 % |
| Phosphatidyléthanolamine (PE) | ≤ 30,0 % | ≤ 30,0 % |
| Phosphatidylcholine (PC) + Phosphatidyléthanolamine (PE) | ≥ 70 % | ≥ 70 % |
| Insolubles dans l'acétone | ≥ 90,0 % | ≥ 90,0 % |
| Insolubles dans l'hexane | ≤ 0,3 % | ≤ 0,3 % |
| Humidité | ≤1,5% | ≤1,5% |
| Solvants résiduels totaux | ≤ 0,5 % | ≤ 0,5 % |
| Indice d'acidité | ≤ 30 mg KOH/g | ≤ 30 mg KOH/g |
| Indice d'iode | ≥ 75 gI/100 g | ≥ 75 gI/100 g |
| Indice de peroxyde | ≤3,0 | ≤3,0 |
| Microorganismes | ||
| PC-50 | PC-70 | |
| Nombre total de bactéries aérobies | ≤100 UFC/g | ≤100 UFC/g |
| Nombre total combiné de levures et de moisissures | ≤100 UFC/g | ≤100 UFC/g |
| Escherichia coli | Négatif/g | Négatif/g |
| Salmonella | Négatif/10g | Négatif/10g |
| Métaux lourds | ||
| PC-50 | PC-70 | |
| métaux lourds totaux | ≤ 20 ppm | ≤ 20 ppm |
| Arsenic (As) | ≤ 2 ppm | ≤ 2 ppm |
| Plomb (Pb) | ≤ 2 ppm | ≤ 2 ppm |
Champ d'application :
| Produits médicaux | La lécithine de soja de qualité pharmaceutique est largement utilisée comme émulsifiant, solubilisant, dispersant pour les préparations orales, ainsi que comme activateur de biodisponibilité et activateur de pénétration locale pour les médicaments oraux. |
Lécithine de soja de qualité pharmaceutique (pour injection) :
La lécithine de soja de qualité pharmaceutique (pour injection) est un produit cireux jaune pâle, fabriqué à partir de lécithine en poudre par extraction à l'éthanol et autres procédés, à l'aide d'équipements brevetés (ZL2017.20049599.7 ; ZL2010.20147413.X). Elle présente de bonnes propriétés d'émulsification, de mouillabilité, d'ajustement de la viscosité, de dispersibilité, d'antioxydants et une activité physiologique unique. Elle est largement utilisée dans les domaines des émulsions injectables, des matières premières pour liposomes et des émulsions fluorocarbonées.
Spécifications du produit :
| Indicateurs physiques et chimiques | ||||
| PC-80 | PC-90 | PC-95 | PC-98 | |
| Apparence | Solide cireux jaune | |||
| Phosphore (P) | ≥ 2,7 % | ≥ 2,7 % | ≥ 2,7 % | ≥ 2,7 % |
| Azote (N) | 1,5%~2,0% | 1,5%~2,0% | 1,5%~2,0% | 1,5%~2,0% |
| Phosphatidylcholine (PC) | ≥ 80 % | ≥ 90 % | ≥ 95 % | ≥ 98 % |
| Phosphatidyléthanolamine (PE) | ≤30% | ≤30% | ≤30% | ≤30% |
| Phosphatidylcholine (PC) + Phosphatidyléthanolamine (PE) | ≥ 80 % | ≥ 90 % | ≥ 95 % | ≥ 98 % |
| Insolubles dans l'acétone | ≥ 90 % | ≥ 90 % | ≥ 90 % | ≥ 90 % |
| Lysophosphatidyléthanolamine (LPE) | ≤1% | ≤1% | ≤1% | ≤1% |
| Lysophosphatidylcholine (LPC) | ≤ 3,5 % | ≤ 3,5 % | ≤ 3,5 % | ≤ 3,5 % |
| Lysophosphatidyléthanolamine (LPE) + Lysophosphatidylcholine (LPC) | ≤ 4,0 % | ≤ 4,0 % | ≤ 4,0 % | ≤ 4,0 % |
| Phosphatidylinositol (PI) | ≤ 5,0 % | ≤ 5,0 % | ≤ 5,0 % | ≤ 5,0 % |
| Total des substances apparentées | ≤8,0% | ≤8,0% | ≤8,0% | ≤8,0% |
| Insolubles dans l'hexane | ≤ 0,3 % | ≤ 0,3 % | ≤ 0,3 % | ≤ 0,3 % |
| Humidité | ≤1,5% | ≤1,5% | ≤1,5% | ≤1,5% |
| Solvants résiduels totaux | ≤ 0,5 % | ≤ 0,5 % | ≤ 0,5 % | ≤ 0,5 % |
| Protéine | Ne devrait pas être détecté | Ne devrait pas être détecté | Ne devrait pas être détecté | Ne devrait pas être détecté |
| Indice d'acidité | ≤ 30 mg KOH/g | ≤ 30 mg KOH/g | ≤ 30 mg KOH/g | ≤ 30 mg KOH/g |
| Indice d'iode | ≥ 75 gI/100 g | ≥ 75 gI/100 g | ≥ 75 gI/100 g | ≥ 75 gI/100 g |
| Indice de peroxyde | ≤3,0 | ≤3,0 | ≤3,0 | ≤3,0 |
| Microorganismes, endotoxines bactériennes | ||||
| PC-80 | PC-90 | PC-95 | PC-98 | |
| Nombre total de bactéries aérobies | ≤100 UFC/g | ≤100 UFC/g | ≤100 UFC/g | ≤100 UFC/g |
| Nombre total combiné de levures et de moisissures | ≤100 UFC/g | ≤100 UFC/g | ≤100 UFC/g | ≤100 UFC/g |
| Escherichia coli | Négatif/g | Négatif/g | Négatif/g | Négatif/g |
| Salmonella | Négatif/10g | Négatif/10g | Négatif/10g | Négatif/10g |
| Endotoxines | <2,0 EU/g | <2,0 EU/g | <2,0 EU/g | <2,0 EU/g |
| Métaux lourds | ||||
| PC-80 | PC-90 | PC-95 | PC-98 | |
| métaux lourds totaux | ≤ 5 ppm | ≤ 5 ppm | ≤ 5 ppm | ≤ 5 ppm |
| Arsenic (As) | ≤ 2 ppm | ≤ 2 ppm | ≤ 2 ppm | ≤ 2 ppm |
| Plomb (Pb) | ≤ 2 ppm | ≤ 2 ppm | ≤ 2 ppm | ≤ 2 ppm |
D'autres spécifications de notre lécithine de soja de qualité pharmaceutique (pour injection) peuvent également être personnalisées en fonction des besoins spécifiques de différents clients.
Champ d'application :
| Produits médicaux | Notre lécithine de soja de qualité pharmaceutique (pour injection) est largement utilisée dans les domaines des préparations injectables, des matières premières liposomales et des émulsions fluorocarbonées. |
Emballage de notre lécithine de soja de qualité pharmaceutique :
1) Tailles :
1 Petits: 10g/sac, 20g/sac, 50g/sac, 100g/sac ou 500g/sac.
2 Les plus grands: 5 kg/carton (1 kg/sac × 5 sacs), 10 kg/carton (1 kg/sac × 10 sacs ou 5 kg/sac × 2 sacs).
2) Matériaux d'emballage :
1 Emballage intérieur :L'emballage intérieur adopte un emballage à double couche : la couche intérieure est un sac en polyéthylène basse densité médicinal et la couche extérieure est un sac en papier d'aluminium ;
2. Emballage extérieur :L'emballage extérieur adopte un emballage à double couche : la couche intérieure est une boîte en mousse avec une glacière intégrée et la couche extérieure est un carton.
Conditions de stockage :
Conserver dans un récipient non ouvert, à l'abri de la lumière et à basse température (inférieure à -18°C).
Durée de conservation :
12 mois à compter de la date de fabrication lorsqu'il est stocké dans les conditions ci-dessus.











![Acide (trans,trans)-[1,1'-bicyclohexyl]-4,4'-dicarboxylique](https://www.handomchemicals.com/uploads/600-300x300.jpg)
